- Porady z zakresu skojarzonego leczenia nowotworów
- Biopsja aspiracyjna cienkoigłowa celowana ( BACC ) piersi, węzłów chłonnych
- Biopsja gruboigłowa guzów tkanek miękkich
- Biopsja wycinkowa guzów nowotworowych
- Biopsja wycinająca guzów nowotworowych
- Wycięcie radykalne zmiany skóry, tkanki podskórnej, piersi
- Elektrokoagulacja zmian tkanek miękkich
- Zeszycie rany
- Drenaż, toaleta ropnia
- USG piersi, jamy brzusznej, tkanek miękkich
- Zabiegi operacyjne tzw. chirurgii krótkoterminowej niewymagające hospitalizacji
Powyższe przykładowe procedury medyczne wykonujemy w naszym gabinecie. Oceny preparatów histologicznych dokonuje zespół doświadczonych patologów w Częstochowie i Kielcach.
.::DIAGNOSTYKA WYBRANYCH NOWOTWORÓW ZŁOŚLIWYCH
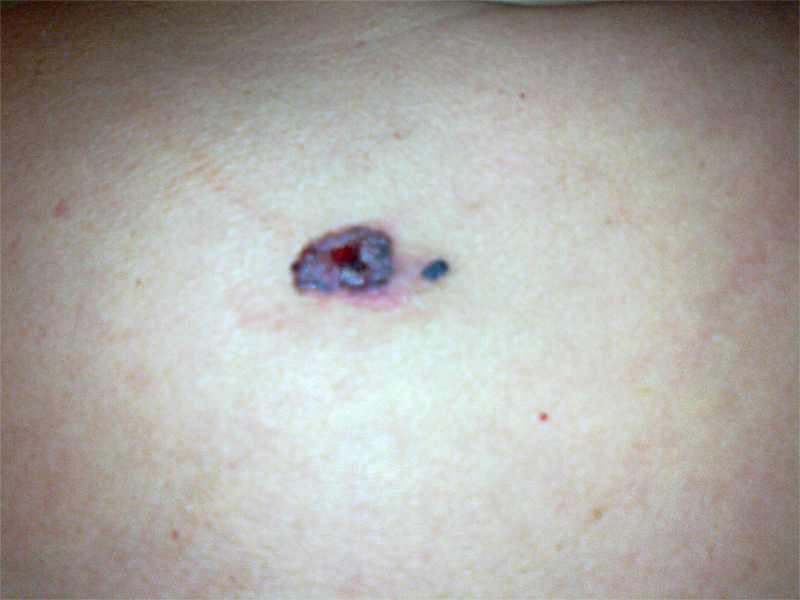
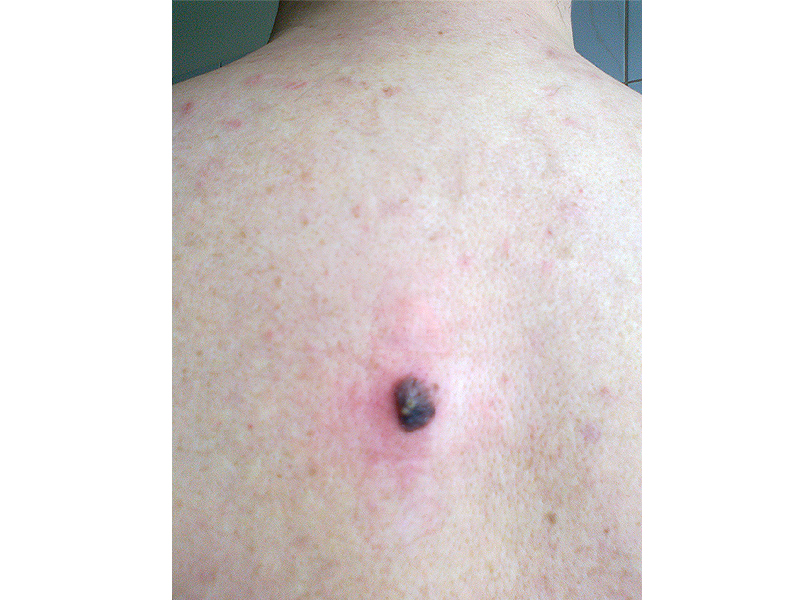
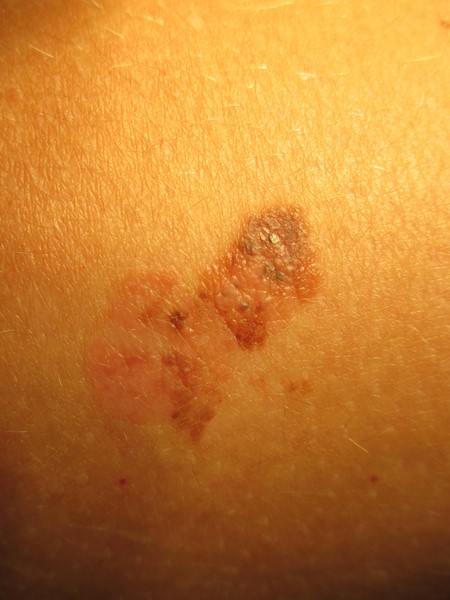
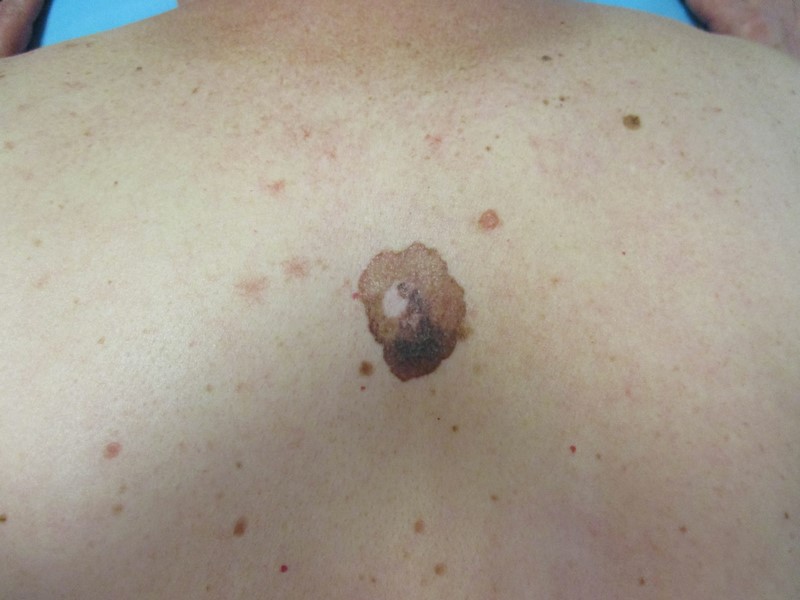
Czerniak skóry ( melanoma malignum ) – rzadki, wyjątkowo złośliwy nowotwór wywodzący się z melanocytów; zapadalność w ciągu ostatnich dekad wyraźnie rośnie ( liczba zarejestrowanych zachorowań w 2005 roku – 2190 osób )
- Wywiad i badanie kliniczne
Podejrzenie czerniaka nasuwają zmiany, które rozwinęły się „de novo„ w okresie obserwacji oraz te, które uległy przemianie. Zastosowanie mają obecnie dwa systemy diagnostyczne opisujące makroskopowe cechy zmiany skórnej:
– system ABCDE; A-asymetry (asymetria), B-borders (brzegi), C-color ( kolor), D-diameter (wymiary), E-elevation (uwypuklenie)
– system Glasgow; 1-powiększanie się zmiany skórnej, 2-zmiana jej kształtu, 3-zmiana koloru, 4-obecność stanu zapalnego, 5-sączenie lub krwawienie ze zmiany, 6-zmiany czucia w okolicy zmiany, 7-rozmiar zmiany powyżej 7mm
- Dermatoskopia
Dzięki oglądaniu zmiany w powiększeniu poprawa czułości diagnostycznej może sięgać 27%
- Biopsja wycinająca
Boczny margines chirurgiczny powinien wynosić 1-3mm niezmienionej chorobowo skóry, w głębi zaś dochodzić do podskórnej tkanki tłuszczowej, powyżej powięzi. Potwierdzenie histopatologiczne czerniaka jest wskazaniem do radykalizacji wycięcia oraz biopsji węzła wartownika lub usunięcia regionalnych węzłów chłonnych.
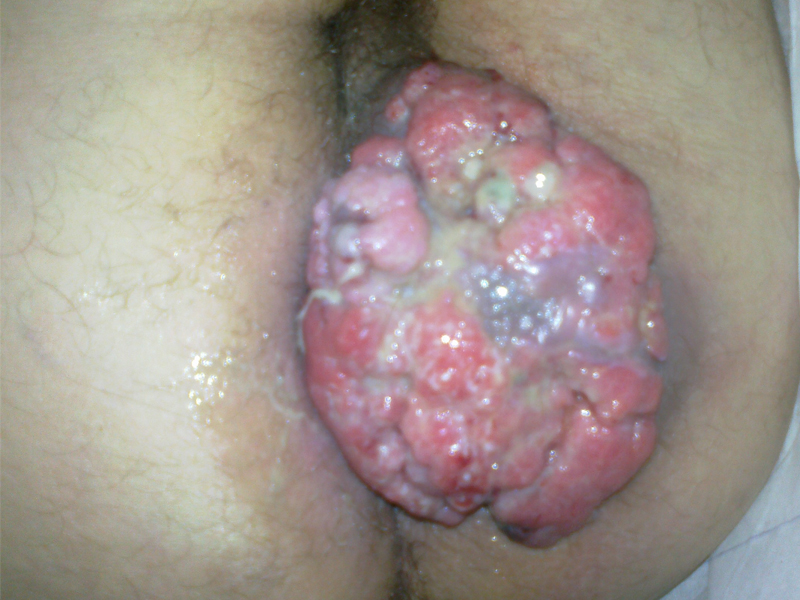
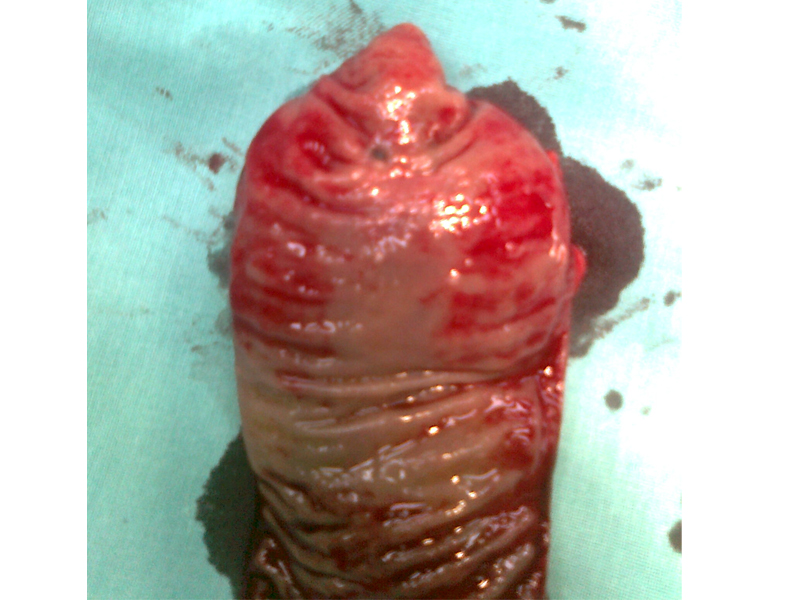
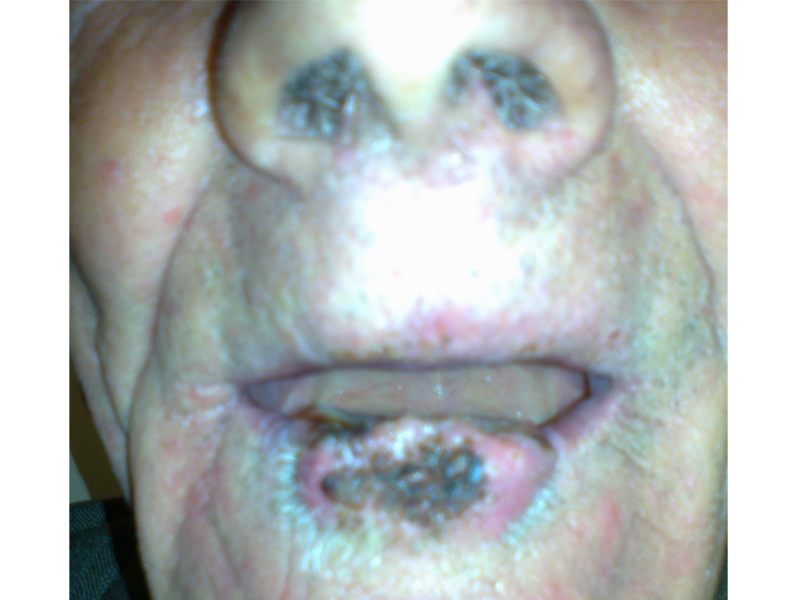
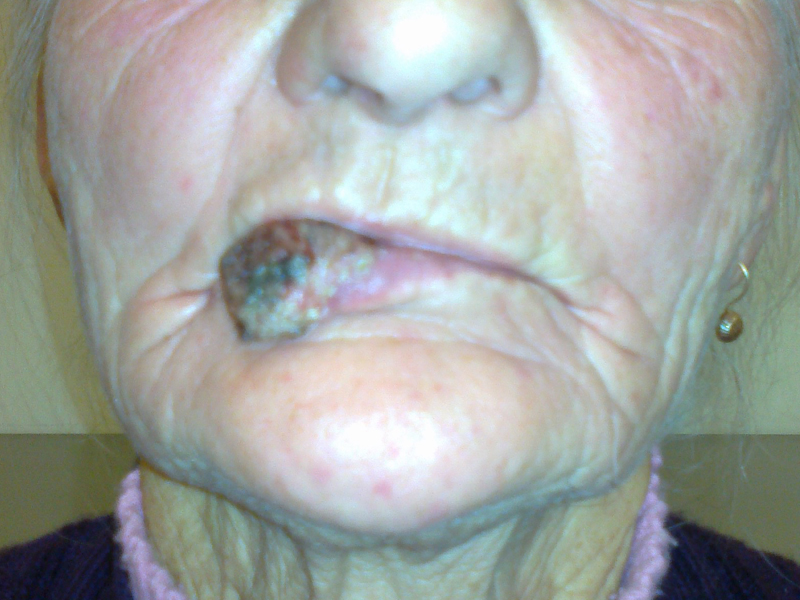
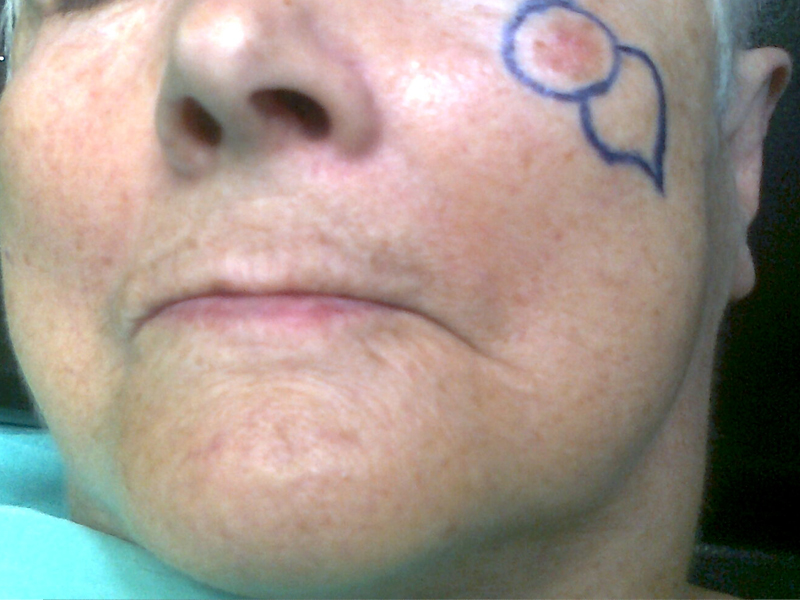
Raki skóry
Rak podstawnokomórkowy ( carcinoma basocellulare ) – stanowi około 75% wszystkich nowotworów skóry. Wyjątkowo rzadko daje przerzuty do regionalnych węzłów chłonnych ale nieradykalne usunięcie ( 5-17% przypadków ) wiąże się z nawrotem miejscowym 33-39%.
Rak płaskonabłonkowy in. kolczystokomórkowy ( carcinoma spinocellulare ) – drugi najczęstszy nowotwór skóry często rozwija się na podłoży zmian popromiennych, przewlekłych ran, blizn pooparzeniowych, owrzodzeń skóry i przewlekłych chorób skóry. Może dawać przerzuty do regionalnych węzłów chłonnych: 10-30% dla raków na podłożu zmian zapalnych, 0.05-16% dla raków bez takiej komponenty.
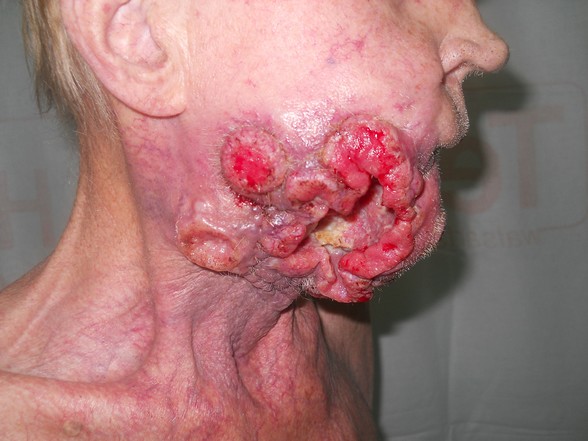
Rak neuroendokrynny skóry ( z komórek Merkla ) – rzadki, złośliwy nowotwór często rosnący na twarzy. Często daje przerzuty do węzłów chłonnych, narządów odległych i nawroty miejscowe ( do 75-80% ).
Diagnostyka raków skóry oprócz wywiadu i badania klinicznego opiera się na:
- biopsji wycinającej ( excisional biopsy )
- biopsji ścinającej ( shave biopsy )
- biopsji punktowej ( punch biopsy )
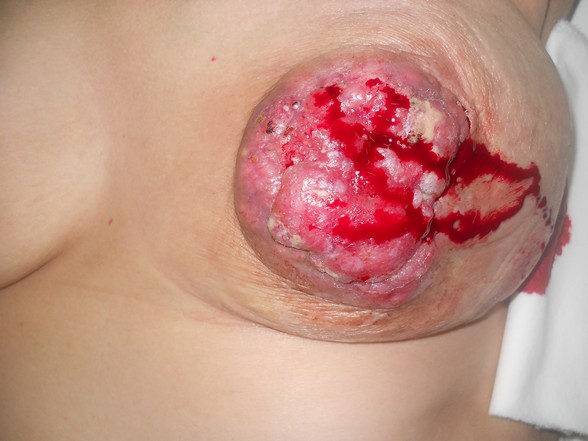
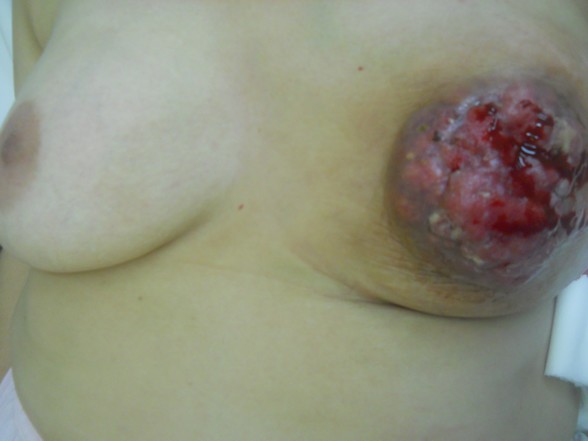
Rak piersi ( carcinoma mammae )
- Badanie podmiotowe: rodzaj dolegliwości ze strony piersi, jago lokalizacja, czas trwania, dynamika, objawy towarzyszące, informacje dotyczące stanu hormonalnego pacjentki, przeszłości położniczo-ginekologicznej, przebytych badań i chorób piersi
- Badanie przedmiotowe: badanie piersi, wygląd skóry ( naciek skóry, obrzęk, owrzodzenie, wygląd skórki pomarańczy, nasilony rysunek naczyniowy ), guz, zmiany w obrębie brodawki ( owrzodzenie, wciągnięcie, wyciek ), badanie węzłów chłonnych, ból piersi, asymetria i cechy zapalenia piersi
- Badania obrazowe: mammografia, usg, rezonans magnetyczny
- Badania patomorfologiczne ( cytologiczne i/lub histopatologiczne )
Biopsja cienkoigłowa celowana ( BACC )
Materiał do badania pobiera się przy użyciu cienkiej igły ( 0.6mm ) i podciśnienia wytworzonego w strzykawce przez osobę pobierającą.
Czułość badania wynosi zaledwie 80-95%. Podczas badania cytologicznego nie jest możliwe odróżnienie raka naciekającego od raka „in situ”.
Rozmaz wycieku z brodawki sutkowej
Czułość badania jest niska ( 40-80% ) dlatego zalecane jest trzykrotne badanie cytologiczne rozmazu
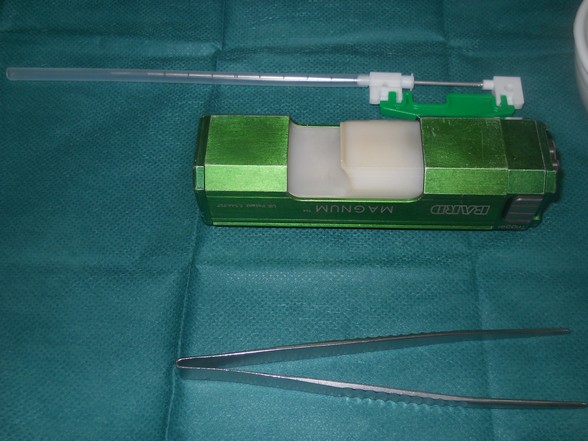
Biopsja gruboigłowa celowana
Grubość igły wynosi zazwyczaj ponad 1.2mm a materiał uzyskany w czasie takiej biopsji umożliwia postawienie rozpoznania histologicznego, odróżnienie raka naciekającego od raka „ in situ” oraz ocenę receptorów estrogenowych, progesteronowych i HER-2.
Biopsja mammotomiczna
W obrębie igły o średnicy ok. 3mm znajduje się wirujące ostrze noża a igła podłączona jest do aparatu próżniowego. Dzięki tej metodzie oprócz wszystkich zalet badania histologicznego ( j.w. ) możliwe jest precyzyjne pobranie tkanek o objętości ok. 2 cm3 i uniknięcie blizny po biopsji chirurgicznej.
Badanie to wykonuje się pod kontrolą usg lub mammografii ( jako tzw. stereotaktyczna biopsja mammotomiczna szczególnie cenna do diagnostyki mikrozwapnień )
Biopsja chirurgiczna
- Biopsja wycinkowa – znajduje zastosowanie w przypadku zmian rozległych kwalifikowanych „ a priori” do leczenia systemowego. W dobie dostępności biopsji gruboigłowej i mammotomicznej znaczenie tej metody maleje. Jej wadą jest pozostawienie blizny, która utrudnia interpretację badań obrazowych u chorych, u których nie potwierdzono raka piersi. Metoda mająca zastosowanie zwłaszcza w przypadku raka Pageta i raka zapalnego
- Biopsja wycinająca ( wycięcie zmiany w piersi w całości ) – ostateczna metoda ustalenia rozpoznania w przypadku niezgodności przeprowadzonych wcześniej badań mikroskopowych, klinicznych i obrazowych. Dla zmian klinicznych oznaczonych w badaniach obrazowych jako BIRADS-5 jest możliwe wykonanie biopsji wycinającej guza bez wcześniejszej biopsji przezskórnej. Obecnie odchodzi się natomiast od śródoperacyjnego badania skrawków mrożonych guza a w przypadku zmian niewyczuwalnych palpacyjnie postępowanie to jest uznane za niewłaściwe ). Biopsja wycinająca zmiany niewyczuwalnej palpacyjnie powinna być poprzedzona jej oznakowaniem ( kotwiczka wkłuta w miejsce guza pod kontrolą mammografii, usg lub rezonansu magnetycznego; radioaktywny znacznik podany w obręb guza i zlokalizowany śródoperacyjnie przy użyciu gammakamery – metoda ROLL ( radio-guided occult lesion localisation ))
Zastosowanie endoskopii w diagnostyce nowotworów przewodu pokarmowego
Gastroskopia
Badanie, w którym dokładnej ocenie poddaje się przełyk, żołądek, opuszkę i część zstępującą dwunastnicy wraz z brodawką Vatera.
Z każdej podejrzanej zmiany pobiera się wycinki do badania histologicznego: z owrzodzenia przełyku min. 8-10 wycinków, z owrzodzenia żołądka min. 6 wycinków, ze zmian przełyku podejrzanych o metaplazję Barretta – liczne wycinki z każdego kwadrantu co 1-2cm.
W wielu ośrodkach rutynowo pobierane są wycinki w celu określenia statusu zakażenia Helicobacter pylori.
Badanie przeprowadza się po ponad 6h okresie głodzenia. Diagnostyczna gastroskopia nie wymaga modyfikacji leczenia przeciwkrzepliwego ani rutynowej profilaktyki antybiotykowej.
Częstość powikłań ocenia się na 0.13% i należą do nich: perforacja ściany, krwawienie, bakteriemia, zaburzenia rytmu serca.
Kolonoskopia
Badanie, które polega na wziernikowaniu dolnego odcinka przewodu pokarmowego giętkim fibroskopem o długości 13-180cm. Badanie wymaga starannego, min. 24h przygotowania ( środki przeczyszczające doustne, wlewki doodbytnicze ). Podobnie jak w gastroskopii nie ma konieczności modyfikacji leczenia przeciwkrzepliwego ani rutynowej profilaktyki antybiotykowej. Wskazania do kolonoskopii:
– potwierdzenie zmiany i pobranie materiału histologicznego w zmianach uwidocznionych radiologicznie
– krwawienia z dolnego odcinka przewodu pokarmowego
– zmiana trybu wypróżnień
– nadzór onkologiczny u pacjentów z wieloletnimi nieswoistymi chorobami zapalnymi jelit ( colitis ulcerosa, choroba Leśniowskiego-Crohna )
– nadzór onkologiczny po leczeniu raka jelita grubego oraz w rodzinach dużego ryzyka rozwoju raka jelita grubego
– oznakowanie lokalizacji nowotworu ( w przypadku zmian małych, niewyczuwalnych śródoperacyjnie )
– badania przesiewowe
Powikłania podobne jak w gastroskopii zdarzają się częściej ( ok. 0.3% badań ) i w zdecydowanej większości są leczone zachowawczo.
Endoskopowa cholangiopankreatografia wsteczna ( ECPW )
Metoda polega na zakontrastowaniu dróg żółciowych i przewodu trzustkowego Wirsunga za pomocą cewnika wprowadzonego przez brodawkę Vatera od strony dwunastnicy pod kontrolą duodenoskopu. Badanie ma na celu wyjaśnienie przyczyn żółtaczki mechanicznej, uwidocznienie nowotworu dróg żółciowych lub trzustki połączone z pobraniem materiału do badania histologicznego i często z zabiegiem leczniczym ( sfinkterotomia, ewakuacja złogów, protezowanie ).
Powikłania występują u 7-10% badanych. Najczęstsze jest ostre zapalenie trzustki i dróg żółciowych a najgroźniejsze krwawienie i perforacja ściany dwunastnicy.
Endosonografia ( EUS )
Metoda wziernikowania górnego lub dolnego odcinka przewodu pokarmowego połączona z badaniem usg struktur i narządów jamy brzusznej dzięki głowicy ultrasonograficznej zamontowanej do końcówki endoskopu.
Badanie to jest szczególnie przydatne do oceny stopnia miejscowego zaawansowania nowotworu ( staging ), diagnostyki zmian w obrębie ściany przewodu pokarmowego lub struktur przylegających. Może być połączone z biopsją pod kontrolą EUS.
Endoskopia kapsułkowa
Metoda polegająca na połknięciu kapsułki wykonującej kilka-kilkanaście zdjęć na sekundę. Służy głównie do oceny jelita cienkiego ( niewyjaśnione krwawienia, guzy, zmiany naczyniowe ). Nie można tą metodą pobrać materiału do badania histologicznego.
Enteroskopia dwubalonowa
Kolejna metoda służąca ocenie jelita cienkiego. Naprzemienne napełnianie dwóch balonów umieszczonych na końcówce enteroskopu oraz rury usztywniającej wprowadzonej od strony jelita grubego poza zastawkę Bauchina umożliwia przesuwanie endoskopu wzdłuż jelita cienkiego. Metoda trudna ale można nią pobrać materiał do badania histologicznego lub wykonać zabieg endoskopowy
Biopsja przezskórna narządów jamy brzusznej
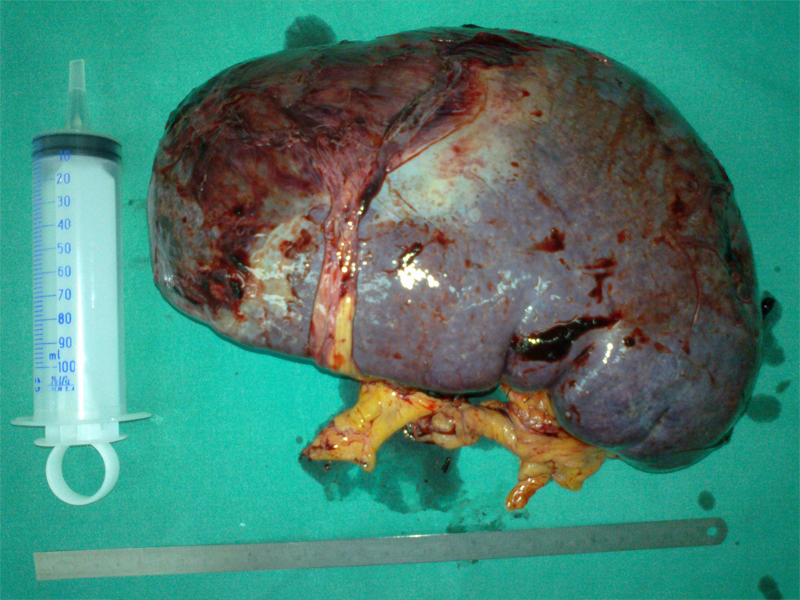
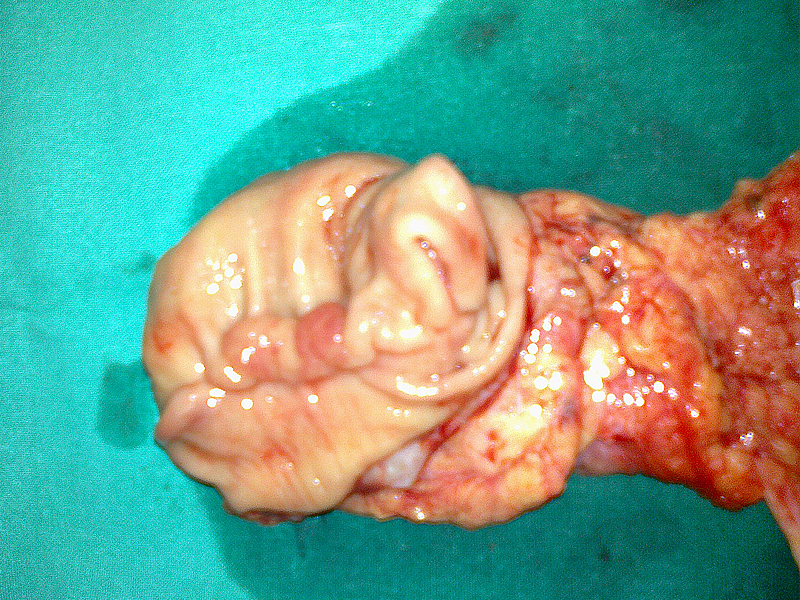
Metoda polegająca na pobraniu adekwatnego materiału z guza jamy brzusznej do badania histologicznego. Badanie wykonuje się po miejscowym znieczuleniu powłok jamy brzusznej przy użyciu igły średnicy ok. 1.2mm typu Trucut pod kontrolą usg. Metoda szczególnie przydatna w przypadku podejrzanych zmian w wątrobie lub trzustce. Czułość diagnostyczna 70-90%. Postawienie rozpoznania na drodze biopsji przezskórnej pozwala podjąć właściwe leczenie bez konieczności diagnostycznego zabiegu operacyjnego.
SPRZĘT:
1. Nowoczesny aparat USG ALOKA HITACHI F37 z zestawem szerokopasmowych głowic: liniową i konweksową plus Doppler.
2. Elektrokoagulacja Valleylab Force EZ
3. Stół zabiegowy Stolter
4. Lampa operacyjna Famed
5. Narzędzia chirurgiczne Aesculap
6. Laser chirurgiczny CO2 Ultra Dream Pulse, Daeshin Enterprise oraz ewakuator dymu DS – 2000E
7. Ligator do gumkowania hemoroidów sposobem Barrona
PERSONEL:
Dr n. med. Grzegorz Celban (specjalista chirurgii ogólnej, specjalista chirurgii onkologicznej)
Lek. med. Paweł Pius (specjalista chirurgii ogólnej, specjalista chirurgii onkologicznej)
Lek. med. Piotr Januszewski (specjalista chirurgii ogólnej, specjalista chirurgii onkologicznej)
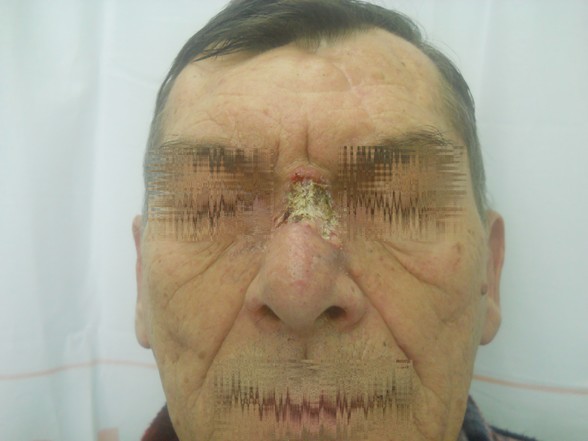

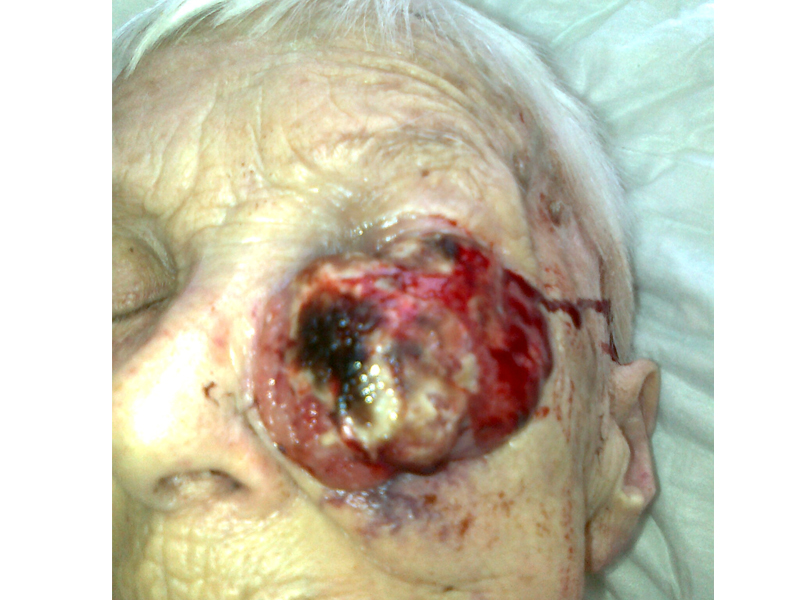
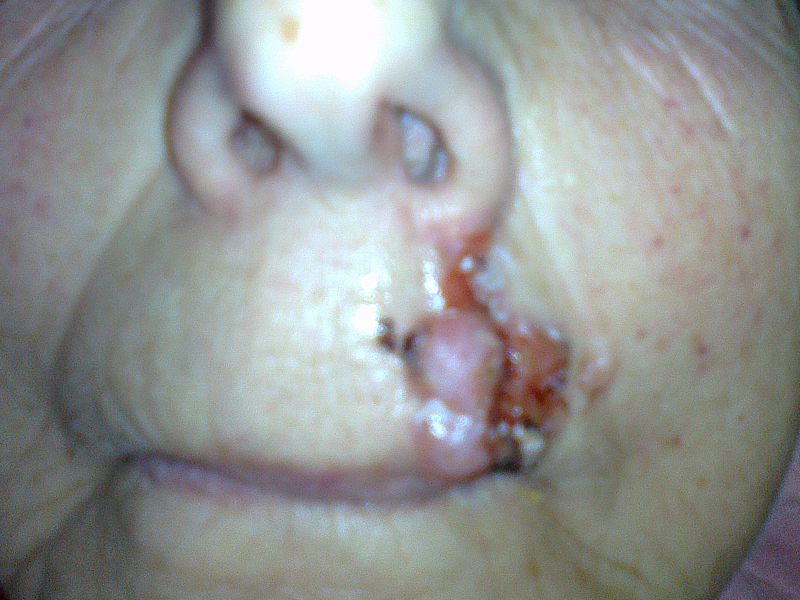
Zaawansowany rak podstawnokomórkowy nosa